Biophysik


Die FG Biophysik erforscht Wirt-Pathogen Interaktionen auf molekularer Ebene. um die zugrundeliegenden Struktur-Funktions-Mechanismen aufzuklären. Wir entschlüsseln und charakterisieren bakterielle und humane Membranen, mit einem besonderen Fokus auf lungenrelevanten Mykobakterien und Gram-negative Bakterien, sowie ihre Interaktionen mit Peptiden und Proteinen. Ein Schwerpunkt liegt auf der Untersuchung neuer Wirkmechanismen membranaktiver Substanzen wie antimikrobieller Peptide und bakterieller Toxine. Unser Ziel ist es nicht nur, Antimikrobielle Resistenz (AMR) zu identifizieren, sondern auch Neue Therapiekonzepte zu entwickeln. Darüber hinaus erforschen wir die Rolle der Membran als äußere Barriere von Bakterien in Bioaktiven Aerosolen. Dabei analysieren wir deren Eigenschaften und entwickeln Methoden zum Nachweis von Pathogenen in Aerosolen.
Ausgehend von biomedizinischen Fragestellungen, die wir häufig in Kooperation mit Partnern am FZB, LCI, CSSB sowie in nationalen und internationalen Netzwerken bearbeiten, setzen wir verschiedene Membranmodelle ein und kombinieren sie mit modernsten biophysikalischen Methoden.
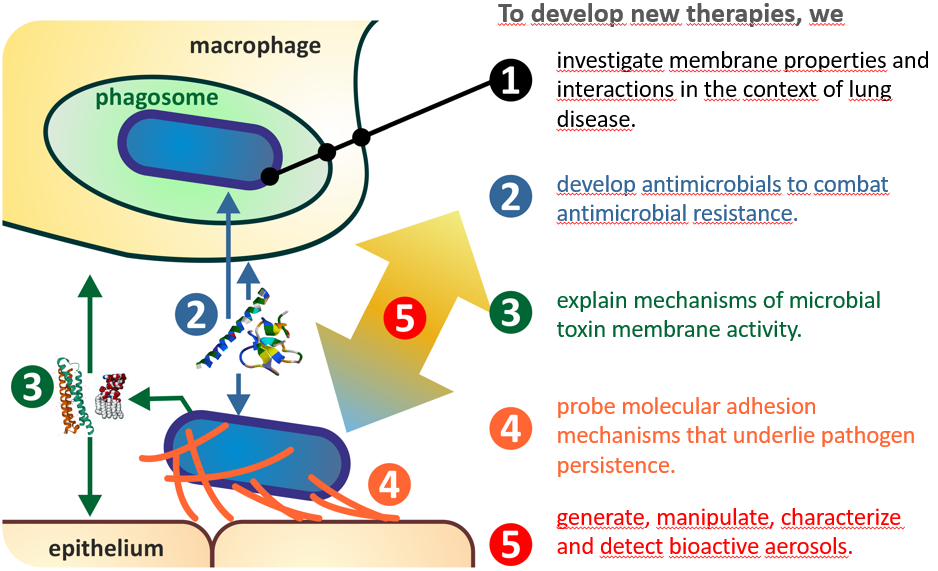
1) Membranstruktur: Die Grundlage aller Untersuchungen ist die Charakterisierung der Lipidmembran. Eine wichtige Rolle spielen dabei die elektrischen und mechanischen Eigenschaften der Membranen sowie ihre laterale und transversale Organisation. Wir untersuchen diese Eigenschaften sowohl an natürlichen Membranen als auch an rekonstituierten Systemen. Um dies zu realisieren, verfügen wir über Expertise in der Aufreinigung von Lipiden aus natürlichen Membranen und der gezielten Rekonstitution von Membranen. Die chemische Charakterisierung erfolgt in Zusammenarbeit mit der FG Bioanalytische Chemie. Mykobakterielle Lipidmembranen spielen die zentrale Rolle in unserem Projekt "Intrazelluläre Membranorganisation in Mycobacterium infizierten Zellen", das Teil des Leibniz-Forschungscampus InterACt ist. Liposomen werden mittels Mikrofluidik gezielt hergestellt und deren Wechselwirkung mit Wirkstoffen charakterisiert.
2) Porenbildende antimikrobielle Substanzen: Wir arbeiten an der Charakterisierung der Funktion von antimikrobiellen Peptiden (AMPs), möglichen Resistenzmechanismen und synergistischen Effekten. Es ist uns gelungen, einen neuen Wirkmechanismus für AMPs zu beschreiben. Die Endotoxin-neutralisierende Aktivität wird nicht nur durch direkte Wechselwirkung der AMPs mit dem Endotoxin erreicht, sondern durch Modifikation der in die Wirtszellmembran eingebauten Rezeptorkomplexe. Gemeinsam mit Partnern entwickeln wir Peptid-basierte neue AMPs mit Spezies-spezifischer Aktivität und ohne zytotoxischen Nebenwirkungen.
3) Mikrobielle Toxine: Membranaktive Peptide können nicht nur gegen Krankheitserreger eingesetzt werden, sondern Mikroorganismen nutzen sie auch gegen menschliche Zellen. Wir untersuchen die Wirkmechanismen des mykobakteriellen ESAT6/CFP10 und anderer WXG-Proteine. Darüber hinaus haben wir in Netzwerken mehrere Kooperationen zur Charakterisierung von z.B. Candidalysin, PLAs und VapA. Insbesondere die Aufklärung der Speziesspezifität spielt hier eine entscheidende Rolle, um zu verstehen, warum AMPs und Toxine trotz sehr ähnliche Wirkmechanismen unterschiedliche Membranstrukturen angreifen.
4) Mikrobielle Adhäsion: Bakterien und andere Mikroorganismen binden durch sehr unterschiedliche Mechanismen an Oberflächen. Bei diesen Oberflächen kann es sich um Wirtszellen oder technische Oberflächen wie z. B. Implantate handeln. Aufgrund unserer Expertise in der Durchführung von Bindungsmessungen arbeiten wir schon seit längerem mit der FG von Iris Bruchhaus am BNITM zusammen, um die Bindung von malariainfizierten Erythrozyten an Epithelzellen zu untersuchen.
5) Infektiöse Aerosole: Ausgehend von einem im Leibniz-Forschungsverbund "Infektionen 21" geförderten Projekts haben wir in den letzten Jahren unsere Expertise auf dem Gebiet der Aerosole deutlich ausgebaut. Zwei Projekte sollen hier kurz genannt werden: a) Dustrisk: In diesem von der Leibniz-Gemeinschaft geförderten Projekt wurde d in einem großen Konsortium gemeinsam mit Forschern aus Leibniz-Instituten und Medizinern auf den Kapverden die Infektiosität von Wüstenstaubpartikeln untersucht. Unser Beitrag war hier die Charakterisierung der Adhäsion von Mikroben an Staubpartikeln. b) Aerofix: Gemeinsam mit der FG "Molekulare und Experimentelle Mykobakteriologie" und dem "Nationalen Referenzzentrum für Mykobakterien" arbeiteten wir an einem von der Else Kröner Fresenius Stiftung geförderten Projekt. In diesem Projekt stellen wir Modellaerosole her, charakterisieren sie und beabsichtigen, gemeinsam mit der Universität Münster ein Graphen-basiertes Sensorsystem für die Diagnostik aufzubauen.
6.) Therapeutische Aerosole: Um die therapeutische Anwendung von AMPs weiter voranzutreiben, haben wir damit begonnen, die Wechselwirkung von Peptiden mit Lipid-Monolayern als Modell der Surfactant-Monolayer in der Lunge zu charakterisieren. Hierzu ist der Aufbau einer Filmwaage mit einem Verneblungssystem notwendig über das bekannte Medikamente appliziert werden können, die im therapeutischen Alltag über die Lunge verabreicht werden. Zusammen mit der Gruppe von Regina Scherließ (Universität Kiel) ist es uns gelungen, ein neues Gerät zur Charakterisierung der mechanischen Stabilität von Medikamentenpellets, die als Aerosol verabreicht werden, zu entwickeln.
|
2025–2029 |
Leibniz Research Alliance Infections; Project title: “Polymicrobial lung infections, interactions with viral pathogens and therapeutic control of biofilms” |
|
2025–2028 |
KIF funding at CSSB; Project title: “TARGET-MYCO – Peptide-Enhanced Targeting and Eradication of Mycobacterium tuberculosis” |
|
2025–2027 |
NHMRC; Project title: “Preclinical validation of anti-tubercular conjugated oligoelectrolytes” |
|
2024–2027 |
Leibniz Collaborative Excellence; Project title: “High-resolution analysis of synergistic effects between membrane-active peptides and classical antibiotics on bacterial membranes” |
|
2024–2027 |
Leibniz Science Campus InterACt; Project title: “Organization of intracellular membrane in Mycobacteria-infected cells” |
|
2022–2027 |
DFG-SPP2332; Project title: “Cytoadherence of Plasmodium-infected erythrocytes” |
|
2024–2026 |
BMBF, DATIpilot Innovation Sprint funding line: “AspidaWund: Anti-infective and anti-inflammatory agent against wound infections” |
|
2023–2026 |
Phospholipid Research Center, Heidelberg: “Liposome-based microfluidic platform for standardized analysis of antibacterial compounds” |
|
2023–2024 |
Start-up Project in the DFG SPP 2225 Exit Strategies of Intracellular Pathogens: “Microfluidic encapsulation of pathogens to study their exit: A bottom-up model system for intracellular compartments” |
|
2021–2023 |
DFG-SPP2225; Project title: “Inside out – The role of mycobacterial ESX secretion systems in phagosome escape” |
|
2020–2023 |
Leibniz Collaborative Excellence; Project title: “A risk index for health effects of mineral dust and associated microbes” |
|
2018–2019 |
Phospholipid Research Center; Project title: “Bottom-up designed synthetic bacteria – a tool to develop new antibiotic strategies” |
|
2015–2020 |
Leibniz Research Alliance Infections’21 |
Membrane reconstitution techniques
-
Small unilamellar liposomes (SUVs)
-
Giant unilamellar liposomes (GUVs)
-
Microfluidic liposome generation
-
Pore-spanning membranes
-
Solid-supported membranes
-
Langmuir–Blodgett transfer
-
Generation of asymmetric lipid membranes
Imaging techniques
-
Atomic force microscopy (at FZB and CSSB, Hamburg)
-
Electron microscopy (at CSSB, Hamburg)
-
Fluorescence microscopy
-
Microfluidics
Electrical techniques
-
Reconstituted planar membranes
-
Impedance spectroscopy on membranes
-
Zeta potential
Protein–lipid interaction techniques
-
Fluorescence spectroscopy
-
Langmuir film balance
-
Lipid State Observer (LISO)
X-ray techniques
-
Reflectivity
-
Small-angle X-ray scattering (SAXS)
-
Grazing-incidence small-angle X-ray scattering (GISAXS)
Aerosol generation and characterization
Lipid and protein purification and characterization
Microbiology and cell biology
-
Antibacterial and cytotoxicity tests
-
Cell culture systems and cytokine induction (ELISA)
2025
Andrä, J, Aisenbrey, C, Sudheendra, US, Prudhon, M, Brezesinski, G, Zschech, C, Willumeit-Römer, R, Leippe, M, Gutsmann, T & Bechinger, B 2025, 'Corrigendum to "Structural analysis of the NK-lysin-derived peptide NK-2 upon interaction with bacterial membrane mimetics consisting of phosphatidylethanolamine and phosphatidylglycerol" [BBA - Biomembranes 1866 (2024) 184267]', BIOCHIMICA ET BIOPHYSICA ACTA-BIOMEMBRANES, S. 184416. https://doi.org/10.1016/j.bbamem.2025.184416
Cronshagen, J, Allweier, J, Mesén-Ramírez, JP, Stäcker, J, Vaaben, AV, Ramón-Zamorano, G, Naranjo-Prado, I, Graser, M, López-Barona, P, Ofori, S, Jansen, PWTC, Hornebeck, J, Kieferle, F, Murk, A, Martin, E, Castro-Peña, C, Bártfai, R, Lavstsen, T, Bruchhaus, I & Spielmann, T 2025, 'A system for functional studies of the major virulence factor of malaria parasites', eLife, Jg. 13. https://doi.org/10.7554/eLife.103542
Rossetti, P, Trollmann, MFW, Wichmann, C, Gutsmann, T, Eggeling, C & Böckmann, RA 2025, 'From Membrane Composition to Antimicrobial Strategies: Experimental and Computational Approaches to AMP Design and Selectivity', Small (Weinheim an der Bergstrasse, Germany), S. e2411476. https://doi.org/10.1002/smll.202411476
2024
Allweier, J, Bartels, M, Torabi, H, Tauler, MDPM, Metwally, NG, Roeder, T, Gutsmann, T & Bruchhaus, I 2024, 'Cytoadhesion of Plasmodium falciparum-Infected Red Blood Cells Changes the Expression of Cytokine-, Histone- and Antiviral Protein-Encoding Genes in Brain Endothelial Cells', MOLECULAR MICROBIOLOGY. https://doi.org/10.1111/mmi.15331
Müller, R, König, A, Groth, S, Zarnowski, R, Visser, C, Handrianz, T, Maufrais, C, Krüger, T, Himmel, M & Lee, S et al. 2024, 'Secretion of the fungal toxin candidalysin is dependent on conserved precursor peptide sequences', Nature Microbiology, Jg. 9, Nr. 3, S. 669-683. https://doi.org/10.1038/s41564-024-01606-z
Nehls, C, Schröder, M, Haubenthal, T, Haas, A & Gutsmann, T 2024, 'The mechanistic basis of the membrane-permeabilizing activities of the virulence-associated protein A (VapA) from Rhodococcus equi', MOLECULAR MICROBIOLOGY, Jg. 121, Nr. 3, S. 578-592. https://doi.org/10.1111/mmi.15233
Gutsmann, T 2024, '"Meet the IUPAB councilor"-Thomas Gutsmann', Biophysical reviews, Jg. 16, Nr. 5, S. 515-517. https://doi.org/10.1007/s12551-024-01226-1
Sae-Ueng, U, Bunsuwansakul, C, Showpanish, K, Phironrit, N, Thadajarassiri, J & Nehls, C 2024, 'Nanomechanical resilience and thermal stability of RSJ2 phage', Scientific Reports, Jg. 14, Nr. 1, S. 19389. https://doi.org/10.1038/s41598-024-70056-8
Schaefer, S, Vij, R, Sprague, JL, Austermeier, S, Dinh, H, Judzewitsch, PR, Müller-Loennies, S, Lopes Silva, T, Seemann, E & Qualmann, B et al. 2024, 'A synthetic peptide mimic kills Candida albicans and synergistically prevents infection', Nature communications, Jg. 15, Nr. 1, S. 6818. https://doi.org/10.1038/s41467-024-50491-x
Schromm, AB, Correa, W, Gisch, N, Steiniger, F, Richter, W, Martinez-de-Tejada, G, Brandenburg, K & von Wintzingerode, F 2024, 'Supramolecular assembly of micellar aggregates is the basis of low endotoxin recovery (LER) in a drug formulation that can be resolved by a whole blood assay', Biomedicine & pharmacotherapy, Jg. 173, S. 116286. https://doi.org/10.1016/j.biopha.2024.116286
2023
Andrä, J, Aisenbrey, C, Sudheendra, US, Prudhon, M, Brezesinski, G, Zschech, C, Willumeit-Römer, R, Leippe, M, Gutsmann, T & Bechinger, B 2024, 'Structural analysis of the NK-lysin-derived peptide NK-2 upon interaction with bacterial membrane mimetics consisting of phosphatidylethanolamine and phosphatidylglycerol', BIOCHIMICA ET BIOPHYSICA ACTA-BIOMEMBRANES, Jg. 1866, Nr. 3, S. 184267. https://doi.org/10.1016/j.bbamem.2023.184267
Donoghue, A, Winterhalter, M & Gutsmann, T 2023, 'Influence of Membrane Asymmetry on OmpF Insertion, Orientation and Function', Membranes, Jg. 13, Nr. 5, 517. https://doi.org/10.3390/membranes13050517
2022
Al Nahas, K, Fletcher, M, Hammond, K, Nehls, C, Cama, J, Ryadnov, MG & Keyser, UF 2022, 'Measuring Thousands of Single-Vesicle Leakage Events Reveals the Mode of Action of Antimicrobial Peptides', ANALYTICAL CHEMISTRY , Jg. 94, Nr. 27, S. 9530-9539. https://doi.org/10.1021/acs.analchem.1c03564
Bachmann, A, Metwally, NG, Allweier, J, Cronshagen, J, Del Pilar Martinez Tauler, M, Murk, A, Roth, LK, Torabi, H, Wu, Y, Gutsmann, T & Bruchhaus, I 2022, 'CD36-A Host Receptor Necessary for Malaria Parasites to Establish and Maintain Infection', Microorganisms, Jg. 10, Nr. 12, S. 2356. https://doi.org/10.3390/microorganisms10122356
Blackler, RJ, Müller-Loennies, S, Pokorny-Lehrer, B, Legg, MSG, Brade, L, Brade, H, Kosma, P & Evans, SV 2022, 'Antigen binding by conformational selection in near-germline antibodies', The Journal of biological chemistry, Jg. 298, Nr. 5, S. 101901. https://doi.org/10.1016/j.jbc.2022.101901
Hansen, J, Kolbe, K, König, IR, Scherließ, R, Hellfritzsch, M, Malm, S, Müller-Loennies, S, Zallet, J, Hillemann, D, Wiesmüller, K-H, Herzmann, C, Brandenburg, J & Reiling, N 2022, 'Lipobiotin-capture magnetic bead assay for isolation, enrichment and detection of Mycobacterium tuberculosis from saliva', PLOS ONE, Jg. 17, Nr. 7, S. e0265554. https://doi.org/10.1371/journal.pone.0265554
Lagune, M, Le Moigne, V, Johansen, MD, Vásquez Sotomayor, F, Daher, W, Petit, C, Cosentino, G, Paulowski, L, Gutsmann, T, Wilmanns, M, Maurer, FP, Herrmann, J-L, Girard-Misguich, F & Kremer, L 2022, 'The ESX-4 substrates, EsxU and EsxT, modulate Mycobacterium abscessus fitness', PLOS PATHOGENS, Jg. 18, Nr. 8, S. e1010771. https://doi.org/10.1371/journal.ppat.1010771
Mogavero, S, Höfs, S, Lauer, AN, Müller, R, Brunke, S, Allert, S, Gerwien, F, Groth, S, Dolk, E, Wilson, D, Gutsmann, T & Hube, B 2022, 'Candidalysin Is the Hemolytic Factor of Candida albicans', Toxins, Jg. 14, Nr. 12, 874. https://doi.org/10.3390/toxins14120874
Möller, C, Heinbockel, L, Garidel, P, Gutsmann, T, Mauss, K, Weindl, G, Fukuoka, S, Loser, D, Danker, T & Brandenburg, K 2022, 'Toxicological and Safety Pharmacological Profiling of the Anti-Infective and Anti-Inflammatory Peptide Pep19-2.5', Microorganisms, Jg. 10, Nr. 12, S. 2412. https://doi.org/10.3390/microorganisms10122412
Palusińska-Szysz, M, Jurak, M, Gisch, N, Waldow, F, Zehethofer, N, Nehls, C, Schwudke, D, Koper, P & Mazur, A 2022, 'The human LL-37 peptide exerts antimicrobial activity against Legionella micdadei interacting with membrane phospholipids', BIOCHIMICA ET BIOPHYSICA ACTA-MOLECULAR AND CELL BIOLOGY OF LIPIDS, Jg. 1867, Nr. 6, S. 159138. https://doi.org/10.1016/j.bbalip.2022.159138
Roeckendorf, N, Nehls, C & Gutsmann, T 2022, 'Design of Membrane Active Peptides Considering Multi-Objective Optimization for Biomedical Application', Membranes, Jg. 12, Nr. 2, 12020180. https://doi.org/10.3390/membranes12020180
Leitung der Forschungsgruppe

Wissenschaftliche Mitarbeiter:innen








Technische Mitarbeiter:innen
Letztes Update: 13.02.2026

